Injertos vasculares regenerativos
Las Enfermedades Cardiovasculares (ECV) son la principal causa de muerte a nivel mundial. ECVs como la ateroesclerosis, aneurismas y la enfermedad vascular periférica atacan los vasos sanguíneos debilitando la pared vascular, obstruyendo o generando una malformación del vaso que resulta en un flujo deficiente. Cuando estas enfermedades se presentan en un estado avanzado, el único tratamiento actualmente disponible es la intervención quirúrgica para la implantación de injertos vasculares autólogos (tomados del mismo paciente) o sintéticos. Sin embargo, ambos presentan problemas en su implementación a largo plazo y comúnmente requieren reintervenciones.
La búsqueda de un injerto que se integre al sistema y responda activamente a las demandas del sistema cardiovascular es una pregunta abierta para la medicina regenerativa y la cirugía cardiovascular. Especialmente, por el bajo desempeño de los injertos sintéticos en condiciones hemodinámicamente complejas como diámetros menores a 5mm o flujos combinados. Trabajamos para el desarrollo de un injerto vascular que promueva la formación de un endotelio saludable en el lumen del injerto y el remodelamiento de la pared vascular mientras evita la oclusión por trombosis.
Estudiamos los mecanismos de endotelialización del cuerpo humano bajo diferentes parámetros hemodinámicos. Contamos con un equipo PIV que permite caracterizar los flujos dentro de diferentes circuitos a través de la toma de imágenes de las partículas dentro del flujo. Desarrollamos biomateriales naturales y sintéticos que caracterizamos mecánicamente haciendo uso de nuestra máquina de tensión biaxial y biológicamente en nuestros laboratorios de cultivo celular. En colaboración con el profesor Juan Carlos Cruz y su grupo de investigación en Nanobiomateriales e Ingeniería Biomolecular trabajamos por funcionalizar las superficies de los injertos para optimizar los procesos de endotelialización y prevención de agregación plaquetaria.
El potencial del injerto de desempeñarse mecánicamente se evalúa de manera dinámica haciendo uso de un simulador endovascular en el que se puede someter al injerto a presiones y flujos equivalentes a aquellos que encontraría una vez implantado. Luego, en conjunto con la profesora Carolina Cruz y su grupo de investigación en ingeniería celular y de proteínas evaluamos el potencial biológico del injerto para promover los procesos de regeneración tisular. Los diseños que muestran mayor promesa se ponen a prueba in-vivo en modelos animales en la sala de cirugía experimental en colaboración con la Fundación Cardioinfantil.
1.1 TEVG
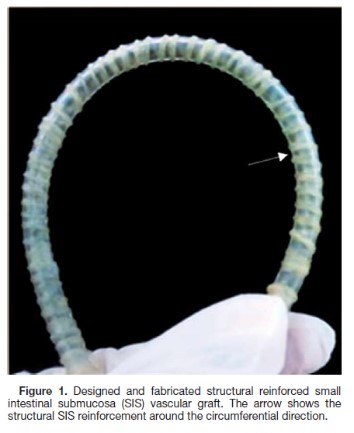
La Ingeniería de Tejidos busca proveer solución a este problema través del diseño de soportes biológicos que se asemejen a las propiedades de los tejidos nativos y promuevan la regeneración del tejido. De esta manera, el Grupo de Ingeniería Biomédica de la Universidad de Los Andes (GIB-UA) ha utilizado con éxito la Submucosa Intestinal Porcina (SIS) para fabricar injertos vasculares regenerativos (TEVG). La composición diversa de la SIS, que es una matriz extracelular rica en colágeno tipo I, factores de crecimiento, proteínas de adhesión y glicosaminoglicanos, provee un soporte óptimo para procesos de regeneración del tejido vascular. Así, el uso de dichos injertos para el reemplazo de aorta en porcinos ha demostrado una regeneración satisfactoria en un 77% de los casos, demostrando la viabilidad de utilizar este material como injerto vascular. Sin embargo, cuando se trata de reemplazar vasos sanguíneos de menor diámetro (< 6 mm) y con geometrías complejas, comprometidos principalmente en enfermedades coronarias, se han evidenciado problemas de permeabilidad y trombogénesis.
Múltiples estudios han demostrado que los TEVGs requieren el recubrimiento de células endoteliales en el lumen del injerto para evitar la adherencia de las proteínas sanguíneas y la subsecuente activación de los mecanismos de coagulación que resultan en la formación de trombos. Con el propósito de entender a mayor profundidad dicha interacción entre material y célula, el GIB-UA ha trabajado en el desarrollo de un biorreactor que permita mimetizar las condiciones dinámicas del ambiente in vivo para el cultivo in vitro de células endoteliales en injertos de diámetro pequeño. A partir de lo anterior, es posible estudiar y caracterizar los injertos vasculares regenerativos desarrollados por el GIB-UA y de esta manera contribuir a la obtención de soluciones ante enfermedades cardiovasculares.
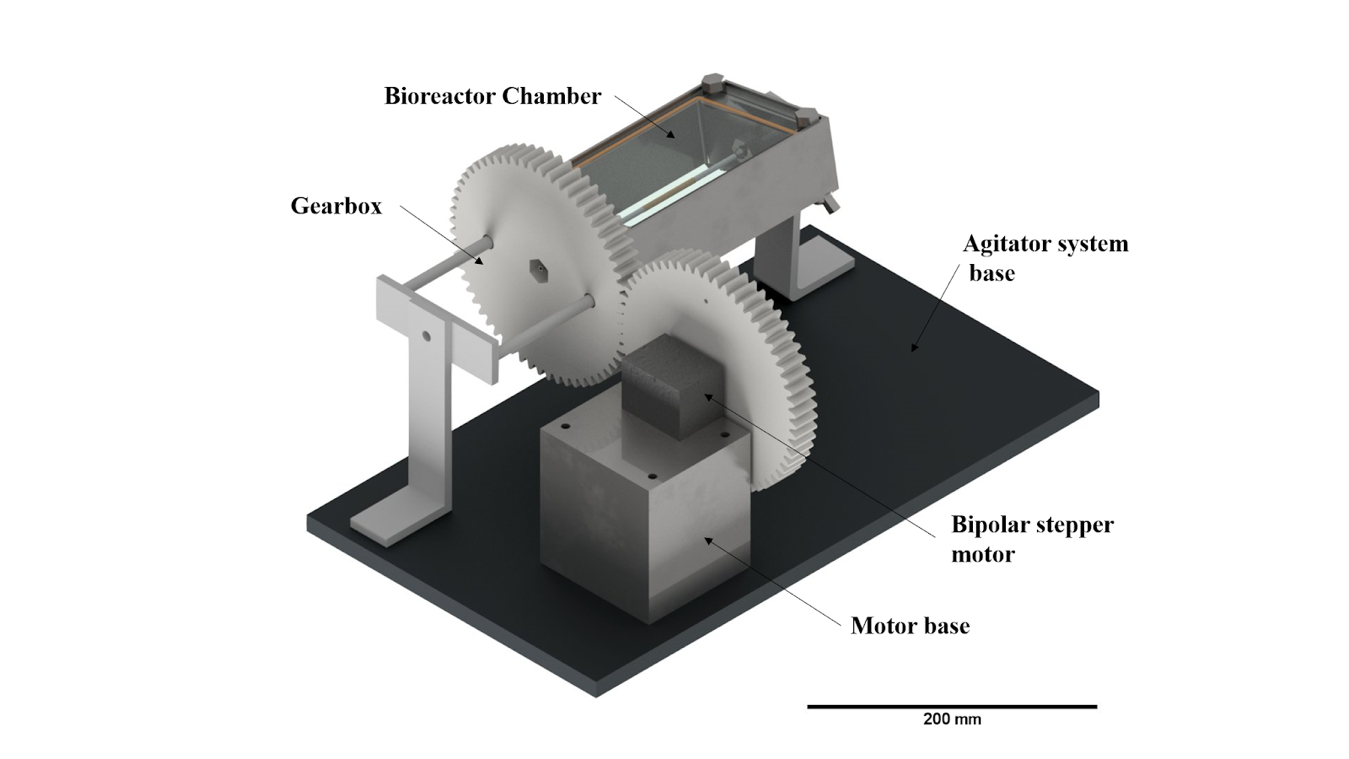
Figura 1. Renderización de ensamble de CADs de los componentes del agitador y el biorreactor.
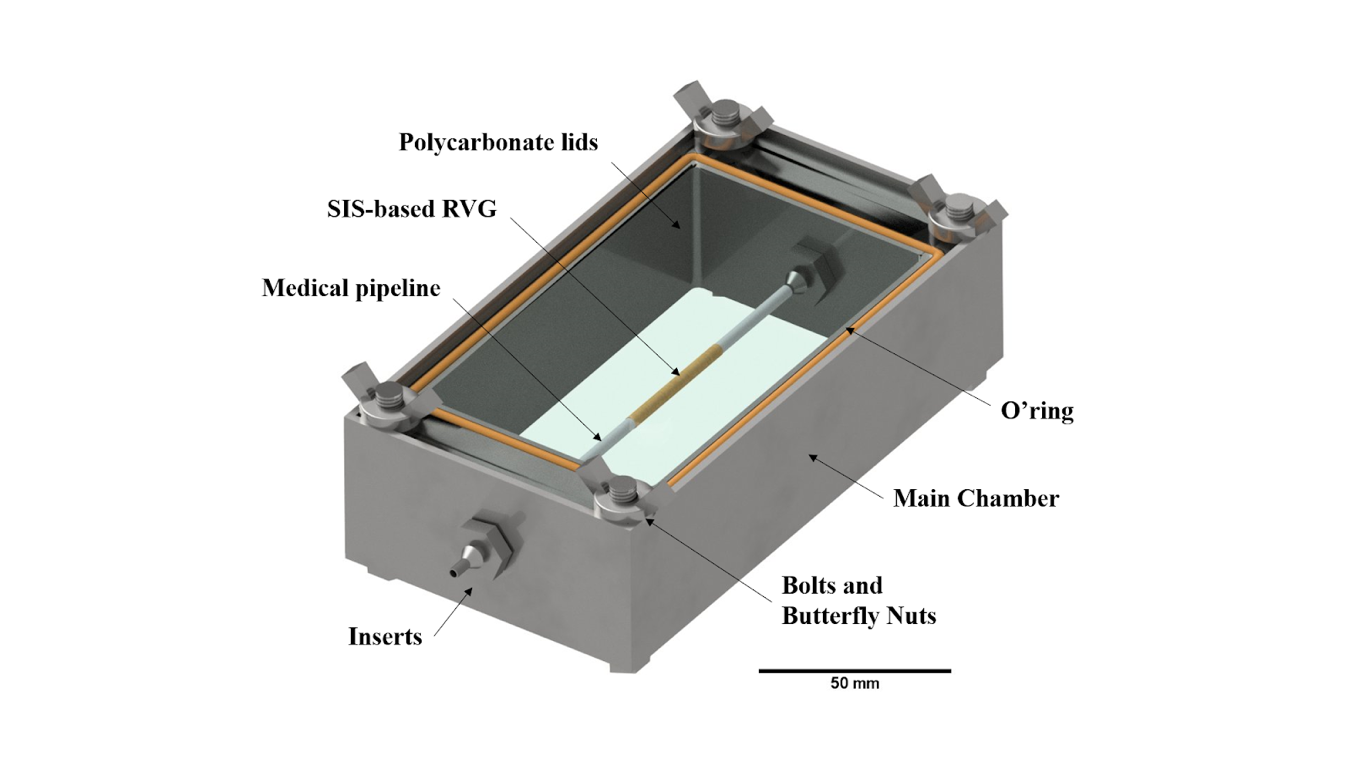
Figura 2. Renderización de los componentes del biorreactor con representación de injerto vascular de Submucosa Intestinal Porcina (SIS).

Figura 3. Proceso de fabricación de injertos de SIS desarrollados en el proyecto A) Injerto tubular B ) Lámina de SIS para fabricación de injertos deshidratada c) Lámina de SIS para fabricación de injertos hidratada.
Financiación
Colciencias código: 277871552208 con contrato 255-2016
Equipos usados
Cabina de flujo laminar, incubadora de células, simulador endovascular (para la evaluación de gradiente de presiones), desarrollo del biorreactor.
Distinciones y productos de innovación
Póster Día de la Investigación FCI 2017, Póster Día de la Investigación FCI 2018, Póster en 1er Congreso Internacional de Ingeniería Biomédica y Bioingeniería, Póster en TERMIS-AM Annual Conference and Exhibition 2019.
1.2. HemodialySIS
El acceso vascular para hemodiálisis es una de las aplicaciones de injertos vasculares en las que los injertos sintéticos disponibles comercialmente no son exitosos debido a que no promueven la re-endotelialización del lumen. Que no haya agregación plaquetaria en el injerto y que este responda de manera adecuada a las condiciones hemodinámicas de la fístula depende de la regeneración adecuada de la capa endotelial y de que esta module apropiadamente la proliferación de las células musculares en la media. Por este motivo, se está trabajando en el diseño de un injerto vascular regenerativo en donde se optimiza la superficie interna para favorecer la adhesión de células progenitoras endoteliales provenientes del flujo sanguíneo. Esta optimización depende de la presencia de péptidos selectivos para la adhesión de progenitoras endoteliales, una topografía alineada en la dirección del flujo que favorezca la deposición de estas células y de que exista continuidad en las propiedades mecánicas del injerto con respecto al vaso nativo para soportar las condiciones de presión y flujo de la fístula.
Como propuestas para el desarrollo de un buen acceso vascular se están considerando una arteria porcina decelularizada y el uso de combinaciones de polímeros con colágeno para ser conformados en forma de tubo a través de electrospinning.
Últimas Publicaciones
• Sánchez, Paolo; Endothelialization mechanisms in vascular grafts; Journal of Tissue Engineering and Regenerative Medicine; 2018
• Valencia, Tatiana; Design and Evaluation of a Structural Reinforced Small Intestinal Submucosa Vascular Graft for Hemodialysis Access in a Porcine Model; ASAIO Journal; 2018
• Valencia, Tatiana; New Regenerative Vascular Grafts for Hemodialysis Access: Evaluation in a pre-clinical animal model; Journal of Investigative Surgery; 2017
Procesos de Innovación
Proceso de Patente iniciado para “Injerto vascular tubular curvo con modificación superficial”
Colaboradores:
Natalia Suarez Vargas, MSc
Asistente graduado de investigación-doctoral
Maria Alejandra Rodriguez Soto, MSc
Asistente graduado de investigación-doctoral
Alejandra Riveros Cortés
Asistente graduado de investigación-maestría
Mónica Cuellar Entrena MSc
Investigadora
Martha Lorena Medina Nieto
Estudiante de maestría
Fidel Enrique Serrano Pacheco
Estudiante de maestría
Andrés García Brand
Estudiante de maestría
Paula Andrea Pinzón Gil
Estudiante de pregrado
Carlos Daniel Cardona Nuñez
Estudiante de pregrado
Tatiana Valencia Rivero, PhD
Estudiante Colaboradora (antigua)
Contacto:
Natalia Suarez Vargas,
Escribirle al correo aquí.
Matrices regenerativas a base de SIS
La submucosa intestinal porcina es un biomaterial que ha demostrado gran potencial en aplicaciones regenerativas por su composición y propiedades mecánicas. En el grupo de investigación hemos desarrollado mecanismos de decelularización y transformación que permiten usar el material en diferentes conformaciones y para diversas aplicaciones.
2.1 Apósitos regenerativos
Desarrollo y caracterización de matrices tridimensionales regenerativas a partir de Submucosa Intestinal Porcina (SIS), ácido hialurónico y quitosano para la re-epitelización de heridas abiertas.
Las heridas crónicas representan un problema de salud pública que afecta aproximadamente a 6.5 millones de pacientes en Estados Unidos. La mayoría de este tipo de heridas, son úlceras asociadas con isquemia, diabetes mellitus, insuficiencia venosa o presión prolongada. Estas no pueden ser sanadas por acción única del cuerpo, debido a la falta de tejido dérmico, lo cual provoca respuesta inflamatoria excesiva que puede conllevar a infecciones o necrosis. Los tratamientos actuales, van desde el uso de terapias avanzadas tales como las terapias de heridas por presión negativa (VAC), hasta el uso de hidrocoloides poliméricos. Sin embargo, estos hidrocoloides fracasan al momento de generar un ambiente celular propicio para llevar acabo los procesos de regeneración.
Es evidente la necesidad de diseñar un apósito que sea biocompatible, biodegradable, con propiedades antibacteriales de ser necesario, que mantenga un microambiente húmedo para promover la regeneración y que pueda adaptarse a diferentes geometrías. Teniendo en cuenta lo anterior, desde la Ingeniería de Tejidos, se ha propuesto el diseño de matrices 3D e hidrogeles a base de Submucosa Intestinal Porcina (SIS), Quitosano (Q) y Ácido Hialurónico como materiales para la regeneración de heridas crónicas. Estas matrices e hidrogeles han sido caracterizados fisicoquímica, mecánica y biológicamente (in vitro e in vivo), con el fin de saber si cuentan con las propiedades necesarias para ser usados como apósitos regenerativos. Actualmente, estamos trabajando en el diseño de un protocolo clínico en pacientes, que será ejecutado en conjunto con la Fundación Cardioinfantil. Alrededor de este proyecto se ha participado en programas de aceleración y desarrollamos estrategias de comercialización de la tecnología para llevarlo al sistema de salud colombiano.
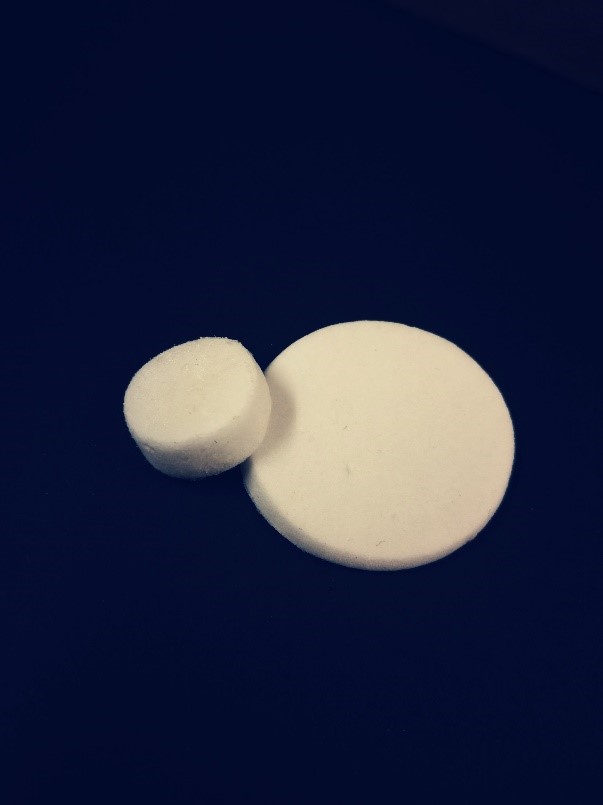
Figura 1. Esponjas de SIS-Q
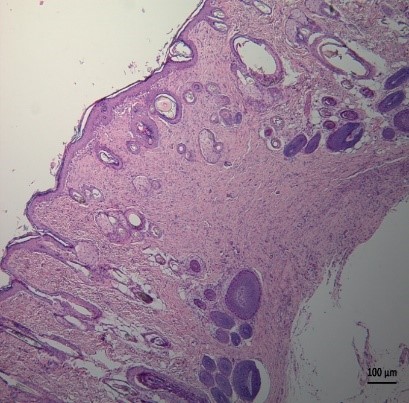
Figura 2. Tinción H&E, explante a los 21 días usando esponja SIS-Q
Financiación:
• Premio día de la investigación 2015 en Fundación Cardioinfantil – Instituto de Cardiología.
• Convocatoria de proyectos interdisciplinarios para estudiantes de pregrado y posgrado 2015 – Universidad de los Andes.
• Convocatoria para proyectos de investigación y desarrollo en ingenierías – 2015 – Departamento Administrativo de Ciencia, Tecnología e Innovación – Colciencias. Contrato No: FP44842-160-2016
Distinciones
• Tercer puesto en el Premio Nacional de Innovación en Dispositivos Médicos – V Foro Internacional de Dispositivos Médicos, Cámara de Dispositivos Médicos e Insumos para la Salud de la ANDI
• Seleccionado dentro de los 15 proyectos para entrar a fase de acompañamiento y aceleración, en desarrollo del programa Oxelerator 2018. Organizado por Oxentia, Colegio de Estudios Superiores de Administración (CESA), Fundación Bolívar Davivienda y Connect Bogotá Región.
Equipos
Los equipos utilizados para el desarrollo de los apósitos son, la cabina de flujo laminar, el molino criogénico y el liofilizador.
Publicaciones
- Artículo en el IX Seminario Internacional de Ingeniería Biomédica (SIB) 2018. “In vitro Biological Evaluation of Small Intestinal Submucosa – Chitosan/Hyaluronic Acid Tridimensional Scaffolds as Deep Wound Healing Dressings”, Jaramillio J, Talero V. A., Cárdenas L. L., Pineda M., Oliveros J. P., Muñoz-Camargo C., Briceño J. C.; 2018 International Seminar of Biomedical Engineering (SIB), Bogotá, 2018, pp.1-9, doi: 10.1109/SIB.2018.8467734.
- Abstract en el congreso anual de la Biomedical Engineering Society (BMES). “Fast Healing of Diabetic Foot Ulcers using SIS-based Regenerative and Antimicrobial 3D Scaffolds”, Cárdenas L. L., Jaramillo J., Muñoz-Camargo C., Cruz J. C., Briceño J. C.; 2018 BMES annual meeting, Atlanta, Georgia, October 17-20, 2018.
- Abstract en el congreso de la Tissue Engineering and Regenerative Medicine Society (TERMIS). “Small Intestinal Submucosa-Chitosan Hydrogel as a Deep Wound Healing Material”. M. Pineda, J. Jaramillo, V. Talero, R. López, C. Muñoz, J. C. Briceño. 2017 Americas Conference & Exhibition Charlotte, NC. December 3-6, 2017.
- Abstract en el congreso de la Tissue Engineering and Regenerative Medicine Society (TERMIS). “In vivo Deep Wound re-epithelialization through Small Intestinal Submucosa/Chitosan Tridimensional Scaffolds”. J. Jaramillo, M. Pineda, V. Talero, R. López, C. Muñoz, J. C. Briceño. 2017 Americas Conference & Exhibition Charlotte, NC. December 3-6, 2017.
- Abstract en el congreso anual de la Tissue Engineering and Regenerative Medicine Society (TERMIS). “Synthesis, physicochemical and mechanical characterization of small intestinal submucosa-chitosan tridimensional scaffolds for deep wound regeneration”, Jaramillo J., Talero V. A., Pineda M., Briceño J. C.; 2016 TERMIS-Americas Conference and Exhibition, San Diego, CA, December 11-14, 2016.
- Abstract en el congreso anual de la Tissue Engineering and Regenerative Medicine Society (TERMIS). “Preparation and physicochemical characterization of small intestinal submucosa-chitosan hydrogels as a new material for tissue engineering applications”, Pineda M., Jaramillo J., Talero V. A., Álvarez O. A., Briceño J. C.; 2016 TERMIS-Americas Conference and Exhibition, San Diego, CA, December 11-14, 2016.
- Abstract en el congreso anual de la Tissue Engineering and Regenerative Medicine Society (TERMIS). “Preliminar in vitro characterization of small intestinal submucosa and hyaluronic acid scaffold as an open wound dressing material”, Talero V. A., Narváez D. M., Jaramillo J., Pineda M., Groot H., Briceño J. C.; 2016 TERMIS-Americas Conference and Exhibition, San Diego, CA, December 11-14, 2016.
- Abstract en el congreso anual de la American Society for Artificial Internal Organs (ASAIO). “Physicochemical and Biological Characterization of Small Intestinal Submucosa Scaffolds for Wound Dressing Applications”. V. A. Talero, D. M. Narváez, H. Groot, R. López, D. M. Tabima, J. C. Briceño. 2016 ASAIO annual meeting, San Francisco, CA June 15-18, 2016.
- Abstract en el congreso anual de la American Society for Artificial Internal Organs (ASAIO). “Synthesis and Physicochemical Characterization of Small Intestinal Submucosa Hydrogels for Deep Wound Regeneration”.M. Pineda, J. Jaramillo, V. A. Talero, O. Álvarez, J. C. Briceño. 2016 ASAIO annual meeting, San Francisco, CA June 15-18, 2016.
Colaboradores Uniandes
Juan Carlos Briceño, PhD
Profesor Titular
Helena Groot, PhD
Profesora Titular
Óscar Álvarez, PhD
Profesor Asociado
Juan Carlos Cruz, PhD
Profesor Asociado
Carolina Muñoz, PhD
Profesora Asociada
Vivian Talero, MSc
Profesora Instructora
Natalia Suárez, MSc
Asistente graduada de investigación-doctoral
Diana Tabima, PhD
Profesora colaboradora (antigua)
Javier Navarro, MSc
Estudiante Colaborador (antiguo)
Mateo Pineda, MSc
Estudiante Colaborador (antiguo)
Juliana Jaramillo, MSc
Estudiante Colaboradora (antigua)
Julieth Oliveros, MSc
Estudiante Colaboradora (antigua)
Jualiana Sanchez, MSc
Estudiante Colaboradora (antigua)
Julián Serna, MSc
Estudiante Colaborador (antiguo)
Lorena Cárdenas
Estudiante Colaboradora (antigua)
Colaboradores Externos:
• Dra. Rocío López, Fundación Santa Fe de Bogotá • Dr. Jorge Ulloa, Fundación Santa Fe de Bogotá • Dra. Olga Cortés, Fundación Cardioinfantil • Dr. Juan Guillermo Barrera, Fundación Cardioinfantil • Enfermera Yudy Andrea Rojas, Fundación Cardioinfantil • Dr. Alejandro Montoya
Contacto
Vivian Talero
Enlace al correo aquí.
2.2 SIGPLUG
Las biopsias percutáneas son una herramienta diagnóstica común para enfermedades hepáticas o renales. Sin embargo, cuando los pacientes presentan afectación en los mecanismos de coagulación, este procedimiento no puede llevarse a cabo y los pacientes deben ser diagnosticados a través de procedimientos más complejos. Se trabaja en el desarrollo de un dispositivo capaz de interrumpir el sangrado después de la biopsia percutánea en pacientes con coagulopatías de tal manera que todos los pacientes puedan ser diagnosticados a través de biopsias percutáneas.
El dispositivo además promueve la regeneración del tejido circundante. Este dispositivo ha pasado pruebas clínicas en pacientes y se está rediseñando para mejorar la interacción de este con el paciente. El desarrollo de este dispositivo implica el diseño de estudios clínicos e interacción con la industria farmacéutica. Alrededor de este proyecto se desarrollan estrategias de innovación y de comercialización de tecnologías de medicina regenerativa para generar impacto en el sistema de salud colombiano. Se trabaja en conjunto con la Fundación Cardoinfantil.
Distinciones
- Premio Innovación en Dispositivos Médicos del V Foro Internacional de Dispositivos Médicos de la ANDI; 2017
Procesos de Innovación
- Patente para “Tapón Hemostático de Matriz Extracelular para Biopsias Percutáneas y su método de Fabricación”
- “BioTexere, a healing company” Modelo de negocio para la comercialización de tecnologías de medicina regenerativa.
Colaboradores
Juan Carlos Briceño
Profesor Titular
Vivian Andrea Talero Niño, MSc
Profesora instructora
Natalia Suarez Vargas, MSc
Asistente graduada de
investigación-doctoral
Javier Navarro, PhD
Estudiante Colaboradora (antigua)
Mateo Pineda, MSc
Estudiante Colaboradora (antigua)
Diana Sánchez, MSc
Estudiante Colaboradora (antigua)
Contacto
Natalia Suárez Vargas
Enlace al correo aquí.
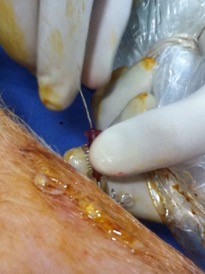
Posicionamiento de SISPlug después de biopsia percutánea de hígado
InnCarddio: innovación en el tratamiento de cardiopatías congénitas ductus Dependientes inspirado en observaciones clínicas y hemodinámicas.
La angioplastia con stents del ductus arterioso en pacientes con atresia pulmonar es un procedimiento mínimamente invasivo que sirve como una intervención paliativa temprana para permitir que el paciente crezca lo suficiente para ser llevado a cirugía correctiva. Es esencial intervenir a estos pacientes temprano durante el período neonatal para evitar complicaciones en la circulación pulmonar y permitir que el paciente crezca y gane peso para que la cirugía correctiva pueda realizarse con menos riesgos. Sin embargo, la canalización del ductus arterioso suele ser difícil debido a la morfología tortuosa que se encuentra en estos pacientes. En InnCarddio desarrollamos el catéter guía en forma de herradura, un dispositivo que permite al cardiólogo intervencionista ingresar al ductus y tener suficiente estabilidad para colocar uno o varios stents a lo largo del conducto. Actualmente, el procedimiento paliativo más común para estos pacientes es la creación de una Fístula Modificada de Blalock-Taussig (MBTS), un procedimiento quirúrgico en el que se crea una unión artificial entre arteria innominada y la arteria pulmonar. Sin embargo, la angioplastia con stent es un procedimiento menos invasivo que permite que los pacientes con menor peso y a una edad más temprana sean intervenidos con resultados clínicos similares. Este proyecto se desarrolla entre la Fundación Cardioinfantil-Instituto de Cardiología y el Departamento de Ingeniería Biomédica de la Universidad de los Andes y se encuentra en fase de ensayo clínico.
Publicaciones
"Stent Angioplasty of the Ductus Arteriosus as an Early Palliative Procedure for Pulmonary Atresia: Single Institution Experience" Juliana Sánchez-Posada, Catalina Vargas-Acevedo, Alberto García Torres, Juan Carlos Briceño Triana. Presentación Oral en ASAIO 64th Annual Conference. Junio 13-16, 2018. Washington DC, USA.
"Stent Angioplasty in Ductal Dependent Pulmonary Blood Flow: Replacing MBTS as Early Palliative Procedure in Tough Ductal Morphology and Complex Cases" Alberto García Torres, Catalina Vargas-Acevedo, Karen Moreno, Juliana Sánchez-Posada, Juan Carlos Briceño Triana, Rodolfo Dennis. Presentación en formato póster en 6th Scientific Meeting of the WSPCHS. Julio 23-26, 2018. Orlando, Florida, USA.
Patente
"Catéter guía en forma de herradura para realizar angioplastia del ductus arterioso en pacientes recién nacidos y lactantes", Certificado número 35015, Resolución No. 17360 del 28 de mayo de 2019.
Financiación
Colciencias, Convocatoria 777 de 2017, contrato 821-2017. Ejecutado por Fundación Cardioinfantil-Instituto de Cardiología, co-ejecutado por Universidad de los Andes.
Equipos usados
El diseño del catéter fue realizado analizando la morfología de los ductus arteriosos de más de 70 pacientes con atresia pulmonar de la FCI-IC. Se realizaron las reconstrucciones 3D de las vasculaturas de 7 pacientes a partir de tomografías utilizando el software de reconstrucción médica Mimics. Los modelos reconstruidos se imprimieron en una impresora 3D Objet 260 Connex 1 de Stratasys utilizando material flexible y translúcido, lo que permitió obtener modelos reales de la vasculatura de los pacientes. Estos se conectan al simulador endovascular para evaluar la funcionalidad del diseño del catéter al intentar acceder al ductus en condiciones dinámicas similares a las de los recién nacidos.
Distinciones y productos de innovación
Consolidación del primer Centro de Impresión 3D Clínico de Colombia en la Fundación Cardioinfantil-Instituto de Cardiología.
Hemosustitutos
Nos ocupamos de la creación de productos para soportar el transporte de oxígeno in vivo, que podrían ser necesarios en situaciones de pérdidas significativas del volumen sanguíneo, como en accidentes, cirugías, y en emergencias. Además trabajamos en el desarrollo de otros productos a partir de perfluorocarbono y de hemoglobina.
Usamos técnicas de preparación y caracterización de los productos que permitan entender su evolución y sus características como sistemas coloidades. También usamos diferentes modelos in vivo para entender su comportamiento antes del uso clínico.
Proyectos en curso:
- Uso de un modeló farmacocinetico del perflurooctil bromuro emulsificado en el choque hemorragico para la prevención de ácidosis lactica.
- Evaluación de una emulsión de perfluorooctil bromuro en el crecimiento de pseudomonas aeruginosa
Póster:
Evaluación de una emulsión de perfluorooctil bromuro en el crecimiento de pseudomonas aeruginosa \ II encuentro de investigación en enfermedades infecciosas.
Colaboradores:
Camila Castro Páez, MSc
Estudiante de Doctorado
Fredy Leonardo Carreño Hernández
Egresado de Medicina de Uniandes
Juliana Sánchez Posada, MSc
Estudiante Colaborador (antiguo)
Contacto:
Camila Castro
Enlace al correo aquí.